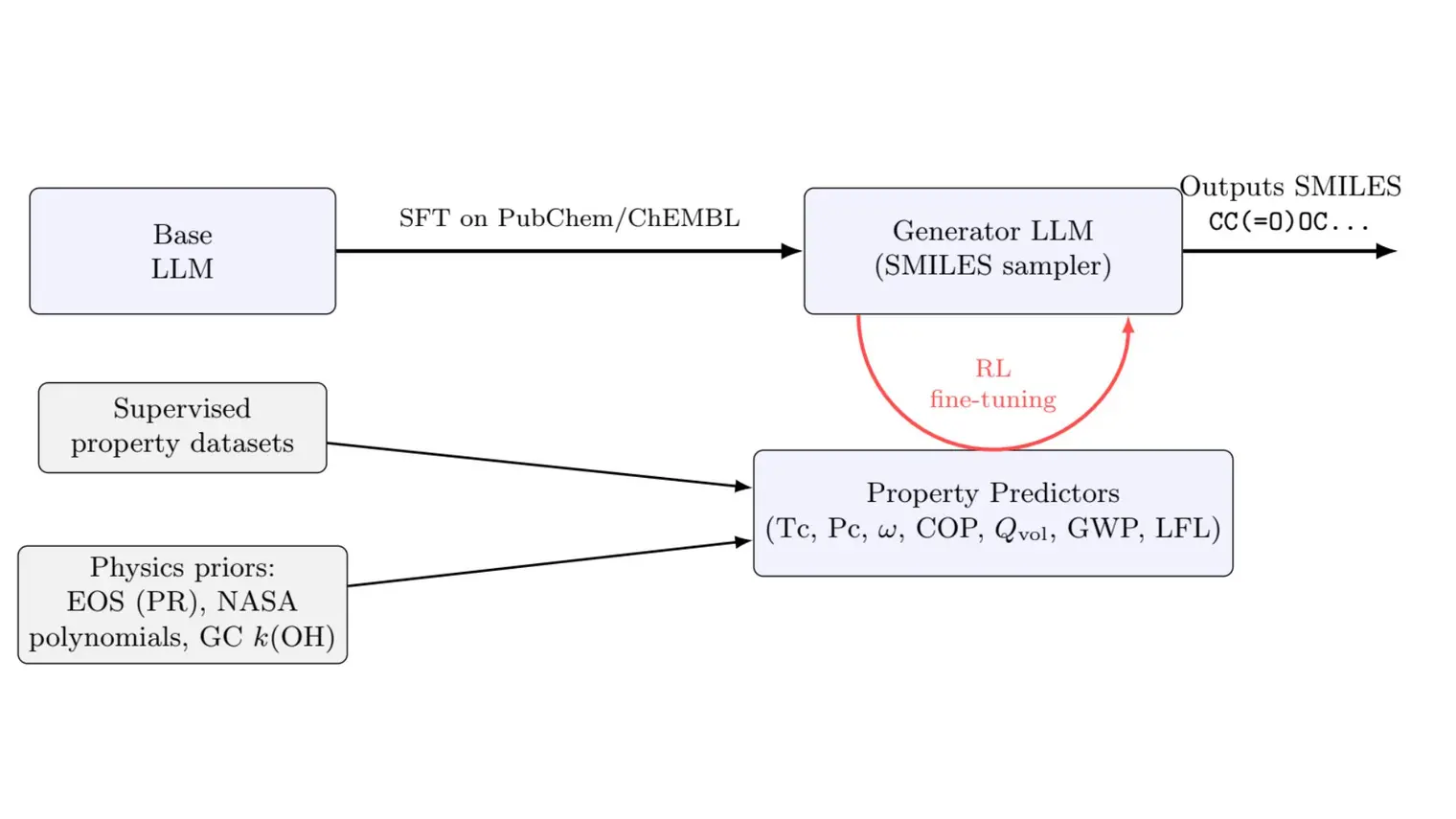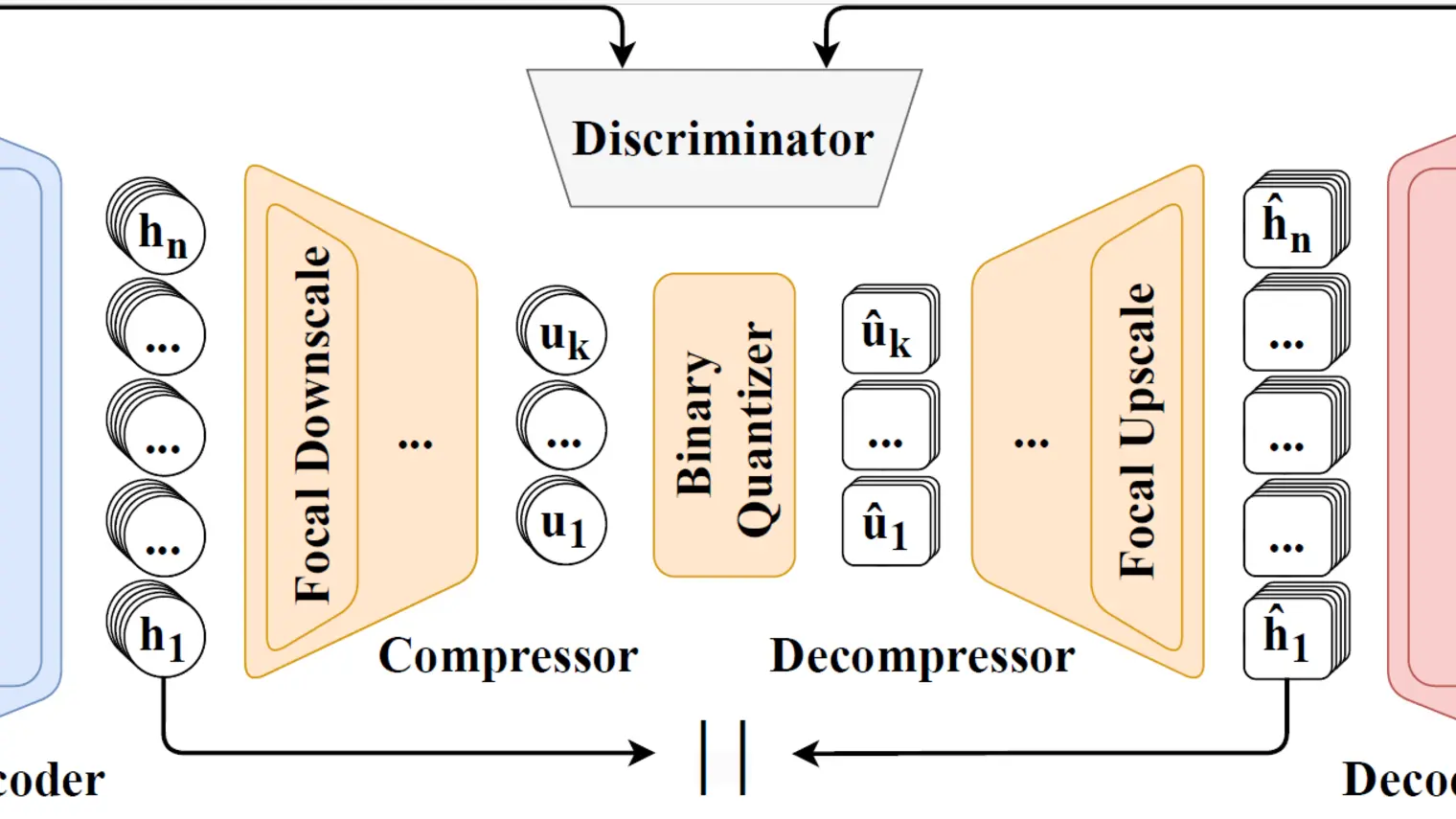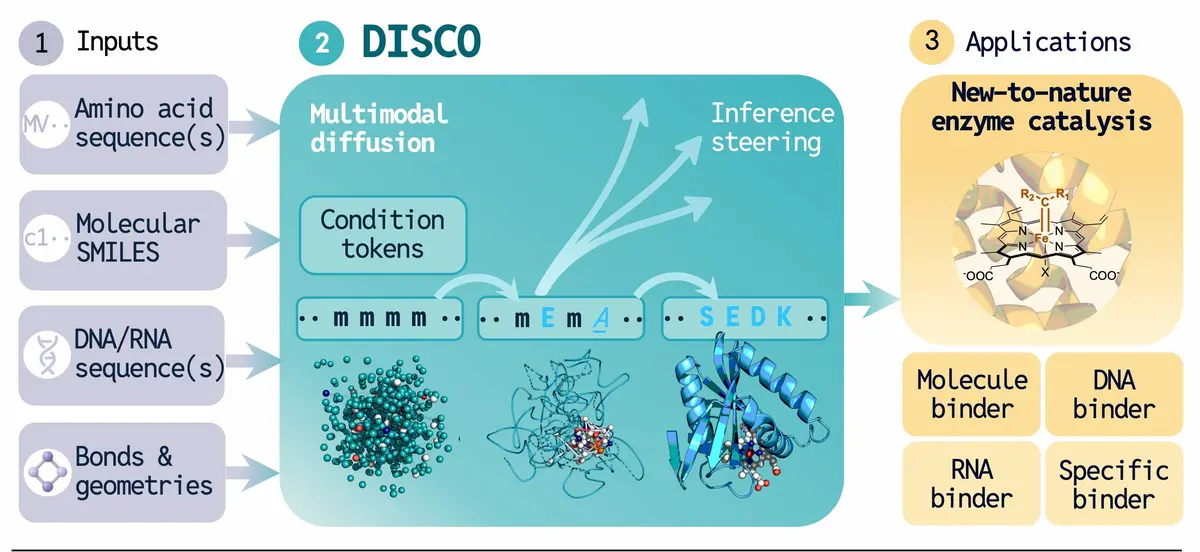
DISCO utilise des plans biologiques, comme l'ADN ou des structures chimiques, pour concevoir simultanément la forme d'une protéine et sa séquence d'acides aminés. Cela permet aux scientifiques de créer des enzymes fonctionnelles inédites dans la nature.
En 2016, une bactérie « mangeuse de plastique » a été découverte dans un centre de recyclage japonais. Cette capacité provient d'une enzyme, une machine moléculaire naturelle capable de tordre, de briser et de fusionner des molécules pour créer de nouvelles substances.
Aujourd'hui, nous pouvons créer de nouvelles enzymes en mutant une enzyme existant déjà dans la nature pour lui donner une nouvelle fonction, ce que l'on appelle l'évolution dirigée. Cependant, cela reste une méthode chronophage, limitée par ce que la nature a déjà inventé.
Les modèles d'apprentissage profond ont réalisé des avancées spectaculaires dans la conception de novo de protéines. Toutefois, l'ingénierie de nouvelles enzymes capables de catalyser des réactions chimiques totalement inédites dans la nature demeure un défi majeur.
Des chercheurs de Mila, Caltech, Aithyra, FutureHouse et leurs collaborateurs présentent aujourd'hui DISCO, un modèle qui élimine ces goulots d'étranglement.
Un modèle unique pour la séquence, la structure et la fonction
La forme d'une enzyme est dictée par sa séquence d'acides aminés, qui l'oblige à se replier dans une structure 3D spécifique. Pour fonctionner, des acides aminés spécifiques doivent être placés de manière stratégique au sein de cette structure. Les modèles conventionnels génèrent d'abord la forme 3D, puis tentent de trouver une séquence correspondante, mais cette déconnexion ne parvient pas à saisir l'interaction complexe entre la chimie et la géométrie. De plus, comme les méthodes actuelles de conception d'enzymes s'appuient sur des plans déjà présents dans la nature, elles peinent à inventer de nouvelles fonctions chimiques.
Contrairement aux processus traditionnels, DISCO conçoit simultanément la séquence d'acides aminés et la structure 3D, ce qui améliore la fidélité. Cela est rendu possible grâce à :
- une fonction de perte multimodale unifiée : une fonction d'objectif unique qui force le modèle à optimiser la séquence et la structure comme une unité inséparable pendant l'entraînement.
- un mécanisme de recyclage intermodal : une boucle de rétroaction itérative où les données de séquence et de structure sont continuellement partagées pour assurer un alignement mutuel parfait.
- une stratégie d'inférence autocorrective : un processus de révision en temps réel qui permet au modèle de détecter et de rectifier les incohérences pendant le processus de génération de l'enzyme.

DISCO génère les complexes enzyme-ligand co-concevables les plus diversifiés pour 178 des 179 cibles dans un nouveau benchmark informatique couvrant diverses molécules naturelles et non naturelles, surpassant toutes les références actuelles.
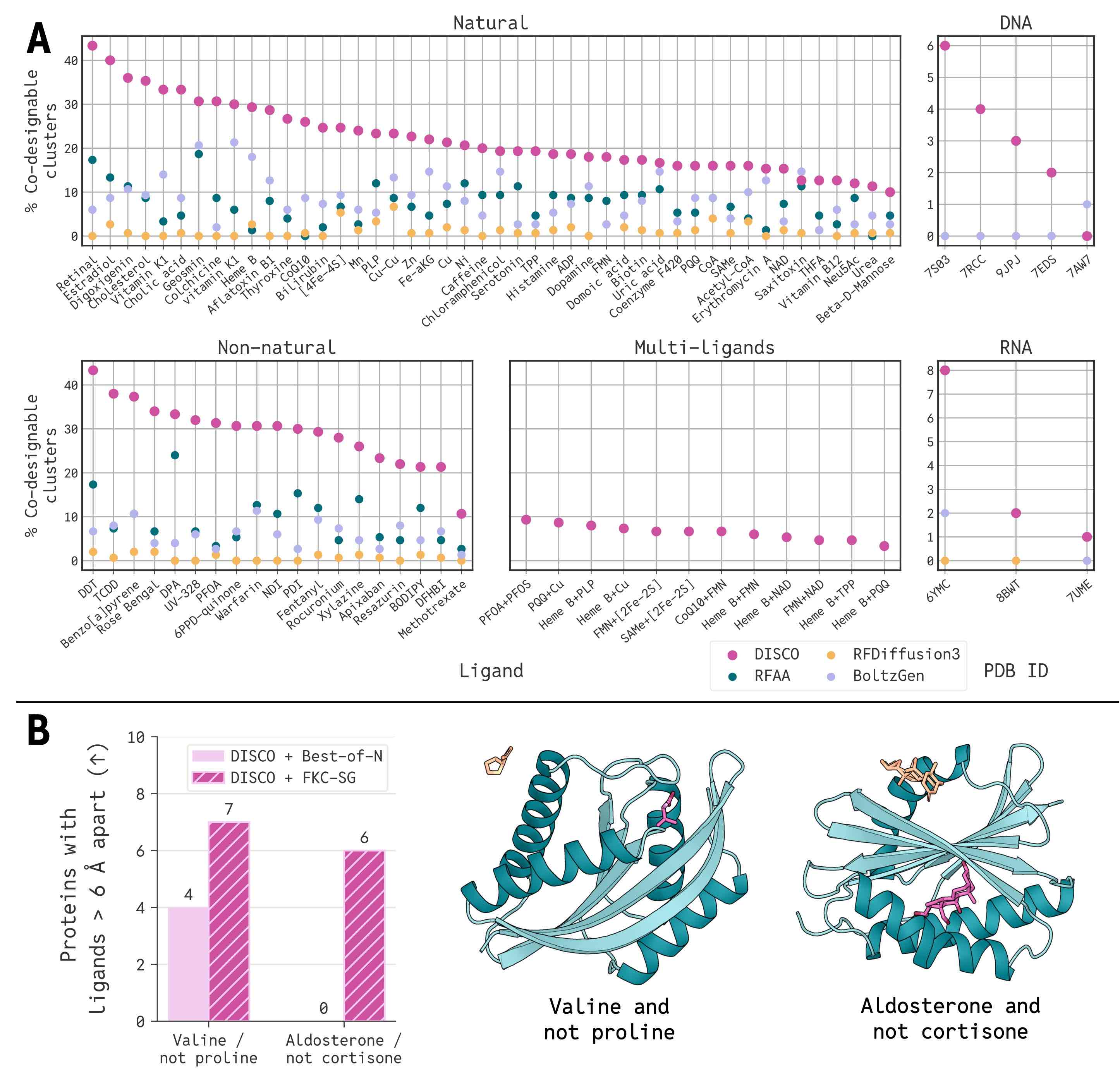
Concevoir des enzymes sans plan préétabli
90 modèles d'enzymes générés par DISCO ont été synthétisés en laboratoire et testés pour leur capacité à catalyser 4 réactions de transfert de carbène, une classe de transformations inédites dans la nature qui se sont révélées précieuses pour la construction de médicaments pharmaceutiques et de molécules complexes :
- Insertion B–H : Cette réaction est totalement étrangère à la biologie. La meilleure conception de DISCO a atteint un rendement de 98 %, avec une seule enzyme répétant la réaction 5 170 fois, faisant plus que doubler l'activité des enzymes précédentes sélectionnées par évolution dirigée.
- Insertion C(sp³)–H : Une fonctionnalisation difficile qui a atteint 2 360 transformations individuelles par enzyme. Cette performance rivalise avec des résultats qui nécessitaient auparavant 14 cycles successifs d'évolution en laboratoire.
- Cyclopropanation d'alcènes : Cette réaction a atteint un rendement de 72 % et plus de 4 000 cycles de réaction par enzyme. Elle a montré une diastéréosélectivité de 99:1 (99 % des molécules produites ont exactement le même arrangement atomique en 3D), surpassant les enzymes pionnières qui ont introduit cette chimie en biologie pour la première fois.
- Spirocyclopropanation : Bien que l'activité initiale ait été modeste, un seul cycle de modifications aléatoires a quadruplé l'efficacité de l'enzyme. Cela a également permis un contrôle précis de la chiralité du produit final. Cette amélioration rapide suggère que ces conceptions sont d'excellents points de départ pour une évolution ultérieure.
Plus important encore, lors d'une comparaison avec la base de données AlphaFold de plus de 200 millions de structures, aucune des enzymes conçues par DISCO ne présentait de géométries de site actif avec des homologues naturels proches. DISCO ne s'est pas contenté de remixer des composants connus ; il a inventé des architectures moléculaires fonctionnelles que l'évolution n'a jamais explorées.
Liens utiles :
- Page du projet : https://disco-design.github.io
- Preprint : https://arxiv.org/abs/2604.05181
- Code : https://github.com/disco-design/disco/