Améliorer l'analyse des images médicales grâce à l'IA
Utiliser l'apprentissage profond pour prédire la réponse au traitement des patients atteints d'une maladie neurologique.
Utiliser l'apprentissage profond pour prédire la réponse au traitement des patients atteints d'une maladie neurologique.
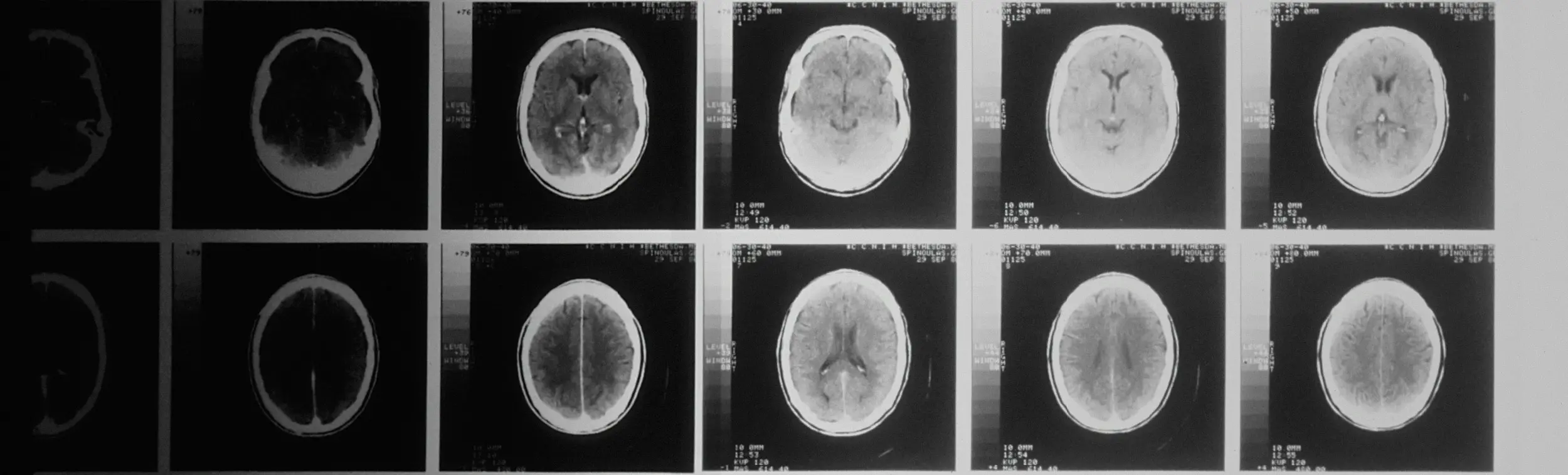
La médecine personnalisée adapte les traitements à chaque patient⋅e et peut s'avérer particulièrement cruciale pour les maladies chroniques telles que la sclérose en plaques (SEP), où un traitement rapide et efficace est essentiel pour prévenir la morbidité et réduire l'invalidité.
Actuellement, les décisions médicales sont fondées sur des statistiques générales et des marqueurs cliniques basés sur la population. Pourtant, utiliser les images de patient⋅e⋅s pour effectuer des prédictions personnalisées peut favoriser des recommandations de traitement tenant mieux compte de l'efficacité des médicaments d'un patient à l'autre.
Cependant, ces modèles d’IA restent sous-explorés et les défis posés par les contextes cliniques entravent leur déploiement en toute sécurité.
Nous développons des modèles d'apprentissage profond analysant des images médicales et destinés aux contextes cliniques et l'amélioration des soins. Par exemple, cela pourrait aboutir à des outils pour aider les médecins à sélectionner les traitements optimaux spécifiques à chaque personne atteinte d’une maladie chronique incurable, ou à une amélioration de l'analyse des essais cliniques.
Nous cherchons à développer des cadres d'apprentissage profond modernes qui prédisent avec précision les résultats futurs des patient⋅e⋅s et les effets des traitements individuels, ce qui requiert de surmonter les défis présentés par les données du monde réel.
Nous devons également garantir la sécurité et la fiabilité des modèles pour assurer un bon déploiement clinique.
Ce modèle permet de prédire avec précision l'aggravation future de la maladie d'un⋅e patient⋅e sous l'effet de toutes les thérapies possibles (et d'un placebo). Nous voulions également identifier les personnes susceptibles de répondre à différents traitements au sein de populations hétérogènes grâce à la prédiction des effets futurs du traitement. Au niveau individuel, cela peut améliorer les recommandations de traitement : ce cadre permet d'identifier des sous-populations de patients répondant aux traitements.
Nous nous efforçons d'améliorer la sécurité et la fiabilité de nos méthodes en élaborant les premiers modèles causaux tenant compte de l'incertitude pour la médecine personnalisée basée sur l'imagerie. La communication de la probabilité de réponse au traitement permettrait de formuler des recommandations plus éclairées.
Nous avons testé le modèle sur un vaste ensemble de données d'essais cliniques de patients atteints de sclérose en plaques, fournies par l'International Progressive MS Alliance.
NeurologyLive s'est entretenu avec Tal Arbel, membre académique associé de Mila, lors du forum ACTRIMS pour en savoir plus sur les travaux réalisés dans ce domaine.
Présentation de Joshua Durso-Finley (McGill/Mila) lors du USS (UNIQUE Student Symposium) dans le cadre d'une session sur la neuroAI dans la recherche médicale.

Aux côtés de mon incroyable équipe de recherche, je suis fière de développer des outils d'IA pour améliorer les perspectives de patient⋅e⋅s atteint⋅e⋅s de maladies incurables.
+1 800
Plus de 1800 patient⋅e⋅s atteint⋅e⋅s de SEP ont été analysé⋅e⋅s dans le cadre de ce projet.
5
Des expériences ont été menées sur 5 traitements différents.
4
Le modèle a été testé dans 4 essais cliniques randomisés.