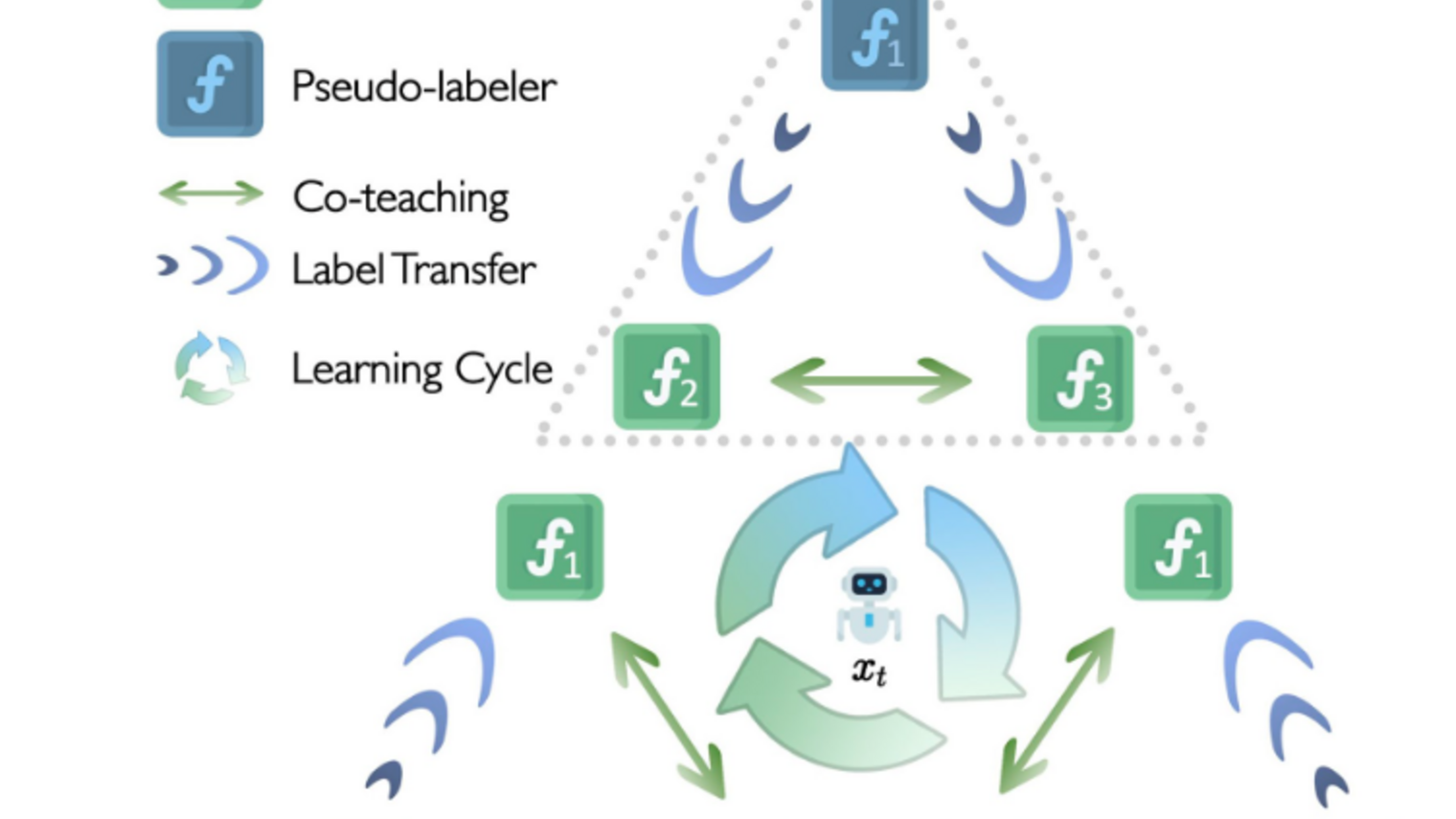
Figure 1. Un exemple d’appareil de radiographie mobile. Crédit image : auntminne
Note de la rédaction : Le travail présenté dans ce billet est en cours d’évaluation par les pairs et a été mis à disposition à des fins de recherche. Il ne doit pas être utilisé pour guider la pratique clinique tant que les résultats d’un essai clinique n’en ont pas vérifié l’efficacité.
Ces derniers mois, la nécessité de rationaliser la prise en charge des patients pour COVID-19 est devenue plus pressante que jamais. La pression grandissante exercée par la pandémie sur les systèmes de santé du monde entier a incité de nombreux médecins à recourir à de nouvelles stratégies et technologies. Une équipe de Mila dirigée par Joseph Paul Cohen, comprenant Lan Dao, Paul Morrison et Yoshua Bengio, ainsi qu’une équipe de l’Institut Vecteur dirigée par Marzyeh Ghassemi, comprenant Karsten Roth, Laleh Seyye-Kalantari et Parsa Torabian, ont œuvré au développement de ces technologies.
Pourquoi les rayons X thoraciques
Les rayons X thoraciques ou radiographies thoraciques (chest X-ray en anglais ou CXR) constituent un outil rapide, non invasif et potentiellement utilisable au chevet des patients (lorsque le système de radiographie est portable) pour suivre la progression de la maladie, en plus d’exposer les patients à des doses de radiation plus faibles que la tomodensitométrie (TDM), qui est un autre outil d’imagerie commun.
Dès mars 2020, certains hôpitaux en Chine ont utilisé l’analyse d’images de tomodensitométrie assistée par intelligence artificielle (IA) pour structurer les soins aux patients atteints par la COVID-19. Depuis, de nombreuses équipes ont lancé des initiatives d’IA pour améliorer le triage des patients COVID-19 positifs, que ce soit pour guider leur congé, leur admission générale ou leur transfert vers l’unité de soins intensifs (USI), de même que l’allocation des ressources, incluant le passage de la ventilation directe non invasive à la ventilation invasive avec respirateur artificiel. Ce n’est que récemment qu’ont fait l’apparition les modèles cliniquement pertinents dérivés de rayons X thoraciques à l’instar de leurs équivalents non basés sur l’imagerie médicale.
Bien que les outils assistés par l’IA puissent être efficaces, ils ne peuvent pas supplanter le jugement clinique. Afin de prévenir l’implantation prématurée d’algorithmes dans les milieux hospitaliers, une évaluation clinique rigoureuse suivant plusieurs axes pratiques s’imposent. À cet effet, des essais cliniques appropriés permettent aux chercheurs d’évaluer avec précision la performance diagnostique de leurs modèles. Même dans l’urgence d’une pandémie, le déploiement de tels outils avant même leur validation clinique ne permet pas d’évaluer s’ils sauvent des vies et améliorent les soins ou, au contraire, s’ils sont nuisibles aux patients et ne confèrent aucun gain net.
Une collaboration intuitive
Le partenariat avec les professeurs Tim Duong et Haifang Li à l’université américaine Stony Brook Medicine permet au Mila d’exercer un fort impact clinique. En tant qu’université doté d’une équipe considérable et affiliée à un hôpital aux premières lignes de la bataille contre la COVID-19, Stony Brook se retrouve dans une position unique pour construire et tester les algorithmes tout en participant aux étapes pour les intégrer dans la pratique clinique telle la création d’étiquettes. De plus, en travaillant avec des données ouvertes, le Mila peut assurer une reproductibilité des résultats et une comparabilité plus grandes avec les résultats d’autres équipes de recherche. Dans un paysage médical où les algorithmes diagnostiques sont progressivement abandonnés au profit d’algorithmes prédictifs, Stony Brook et Mila Medical s’efforcent d’instaurer notre modèle prédictif dans un cadre clinique. Cela permettrait de réduire les risques de sur-ajustement et de biais et ainsi estimer les performances avec précision.
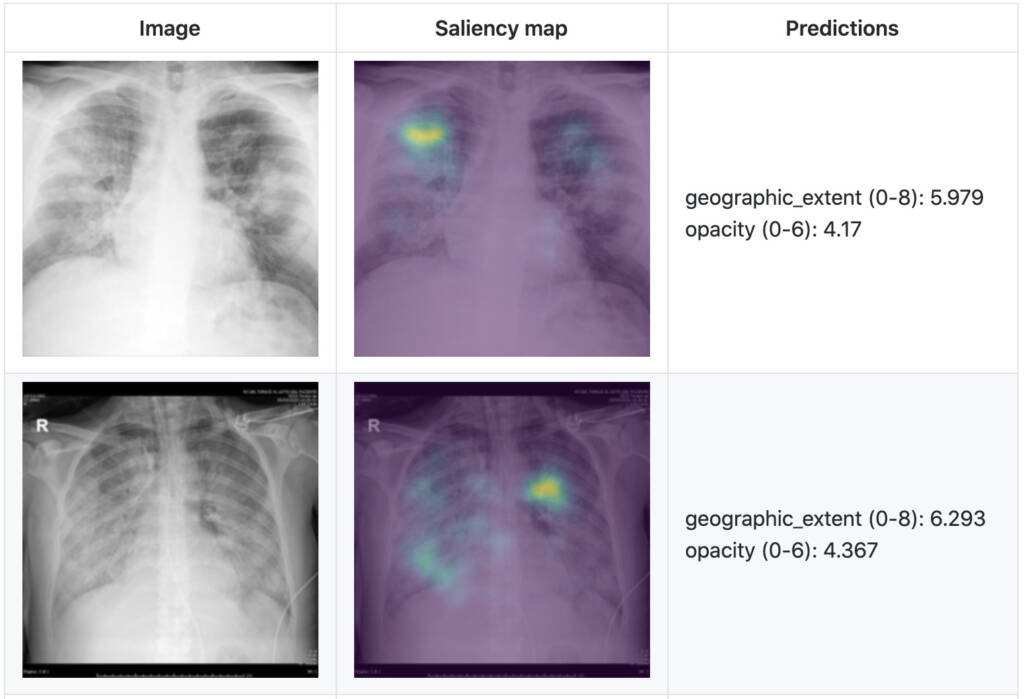
Dans une étude récente, tel qu’illustré par la Figure 2, nous présentons un modèle prédictif (pas encore destiné à l’usage médical) du score de gravité de la pneumonie COVID-19 pour les radiographies postéro-antérieures (PA) du thorax, développé à partir de notre base de données ouverte de rayons X thoraciques de patients COVID-19 positifs. Cette étude démontre que l’entraînement d’un modèle de régression sur un sous-ensemble de sorties d’un modèle pré-entraîné à partir de radiographies thoraciques permet de prédire notre score d’étendue géographique (plage 0-8, 8 étant plus sévère) avec une erreur absolue moyenne (EAM) de 1,14 et notre score d’opacité pulmonaire (plage 0-6, 6 étant plus sévère) avec une EAM de 0,78. Un tel outil permet d’évaluer la gravité de la pneumonie COVID-19, qui peut être utilisé pour l’ajustement des soins ainsi que pour le suivi de l’efficacité du traitement, notamment dans l’unité de soins intensifs (USI).
Un complément à la prise en charge clinique
Les radiographies thoraciques des patients pourraient être mesurées régulièrement après le diagnostic afin de suivre l’évolution de la maladie et la réponse au traitement. Éventuellement, ces images utilisés pour le suivi pourraient être téléchargés dans notre base de données, permettant à des chercheurs de concevoir des outils prédictifs et de mieux comprendre le rétablissement. Le score de gravité développé par le Mila et Stony Brook pourrait également être utilisé comme instrument objectif et quantitatif afin d’étudier la réponse à divers traitements ou algorithmes de gestion et inspirer de meilleures stratégies en clinique.
Notamment, la prise en charge des patients dans les USI pourrait être assistée par un modèle prédisant la gravité de la pneumonie COVID-19 et de la pneumonie en général à partir de rayons X thoraciques. Cette idée a déjà explorée par d’autres équipes qui ont utilisé des méthodes autres que l’apprentissage profond pour créer un modèle prédictif basé sur des scores pour le transfert aux USI combinant les informations provenant d’images de tomodensitométrie ou de radiographies thoraciques avec des données cliniques non liées à l’imagerie médicale.
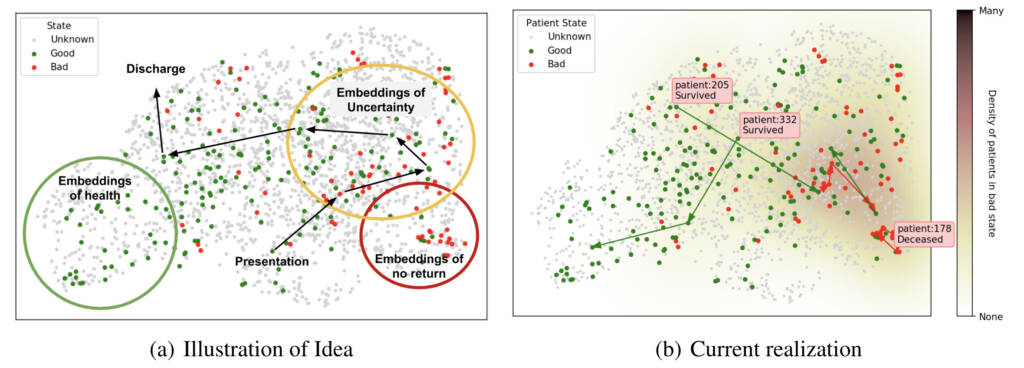
En supposant représentation suffisamment expressive, les patients pourraient être tracés comme le montre la Figure 3, qui présente une illustration conceptuelle (Figure 3a) de même que notre réalisation actuelle (Figure 3b). Ces images ont été créées à l’aide d’un modèle pré-entraîné à l’aide de rayons X thoraciques et présentent des exemples de trajectoires pour les patients. Une telle approche pourrait nous permettre d’explorer les représentations apprises en itérant rapidement avec une équipe médicale pour donner un sens aux complexités du modèle et des patients.
Nos prochains efforts de recherche seront consacrés à l’amélioration du modèle prédictif pour inclure la trajectoire.
Vers le déploiement
Grâce aux travaux initiaux de révision par les pairs, nous avons mis notre prototype à disposition pour essai (et non pour un usage médical) dans la bibliothèque TorchXrayVision. Nous espérons que de nombreux groupes évalueront ce modèle afin de déterminer s’il est efficace. Pour permettre un travail de suivi, nous mettons notre code, nos étiquettes et nos données à disposition en ligne.
Ce billet de blogue est basé sur notre publication récente:
Predicting COVID-19 Pneumonia Severity on Chest X-ray with Deep Learning
Joseph Paul Cohen, Lan Dao, Paul Morrison, Karsten Roth, Yoshua Bengio, Beiyi Shen, Almas Abbasi, Mahsa Hoshmand-Kochi, Marzyeh Ghassemi, Haifang Li, Tim Q Duong
arXiv:2005.11856
Code: https://github.com/mlmed/torchxrayvision/tree/master/scripts/covid-severity
Remerciements
Nous tenons à remercier l’Institut canadien de recherches avancées (ICRA) pour sa subvention Catalyseur IA-COVID-19.
Références
Gozes, O., Frid-Adar, M., Greenspan, H., Browning, P. D., Zhang, H., Ji, W., Bernheim, A., & Siegel, E. (2020). Rapid AI Development Cycle for the Coronavirus (COVID-19) Pandemic: Initial Results for Automated Detection & Patient Monitoring using Deep Learning CT Image Analysis. ArXiv:2003.05037 [Cs, Eess]. http://arxiv.org/abs/2003.05037
Strickland, E. (2020). AI Can Help Hospitals Triage COVID-19 Patients. IEEE Spectrum. https://spectrum.ieee.org/the-human-os/artificial-intelligence/medical-ai/ai-can-help-hospitals-triage-covid19-patients
Wittbold, K. A., Carroll, C., Iansiti, M., Zhang, H. M., & Landman, A. B. (2020). How Hospitals Are Using AI to Battle Covid-19. Harvard Business Review. https://hbr.org/2020/04/how-hospitals-are-using-ai-to-battle-covid-19
Toussie, D., Voutsinas, N., Finkelstein, M., Cedillo, M. A., Manna, S., Maron, S. Z., Jacobi, A., Chung, M., Bernheim, A., Eber, C., Concepcion, J., Fayad, Z., & Gupta, Y. S. (2020). Clinical and Chest Radiography Features Determine Patient Outcomes In Young and Middle Age Adults with COVID-19. Radiology, 201754. https://doi.org/10.1148/radiol.2020201754
Borghesi, A., Zigliani, A., Golemi, S., Carapella, N., Maculotti, P., Farina, D., & Maroldi, R. (2020). Chest X-ray severity index as a predictor of in-hospital mortality in coronavirus disease 2019: A study of 302 patients from Italy. International Journal of Infectious Diseases, 96, 291–293. https://doi.org/10.1016/j.ijid.2020.05.021
Wynants, L., Van Calster, B., Collins, G. S., Riley, R. D., Heinze, G., Schuit, E., Bonten, M. M. J., Damen, J. A. A., Debray, T. P. A., De Vos, M., Dhiman, P., Haller, M. C., Harhay, M. O., Henckaerts, L., Kreuzberger, N., Lohmann, A., Luijken, K., Ma, J., Andaur Navarro, C. L., … van Smeden, M. (2020). Prediction models for diagnosis and prognosis of covid-19: Systematic review and critical appraisal. BMJ, m1328. https://doi.org/10.1136/bmj.m1328
Cohen, J. P., Dao, L., Morrison, P., Roth, K., Bengio, Y., Shen, B., Abbasi, A., Hoshmand-Kochi, M., Ghassemi, M., Li, H., & Duong, T. Q. (2020). Predicting COVID-19 Pneumonia Severity on Chest X-ray with Deep Learning. https://arxiv.org/pdf/2005.11856.pdf
Cohen, J. P., Morrison, P., & Dao, L. (2020). COVID-19 Image Data Collection. https://arxiv.org/abs/2003.11597
Cohen, J. P., Morrison, P., Dao, L., Roth, K., Duong, T. Q., & Ghassemi, M. (2020). COVID-19 Image Data Collection: Prospective Predictions Are the Future. https://arxiv.org/abs/2006.11988
Cohen, J. P., Viviano, J., Hashir, M., & Bertrand, H. (2020). TorchXRayVision: A library of chest X-ray datasets and models. https://github.com/mlmed/torchxrayvision